Nghiên cứu khoa học: Ảnh hưởng của quá trình khử trùng bằng tia UV và bức xạ gamma đối với các hạt nano polyme khác nhau cho các ứng dụng y sinh (Phần 1)
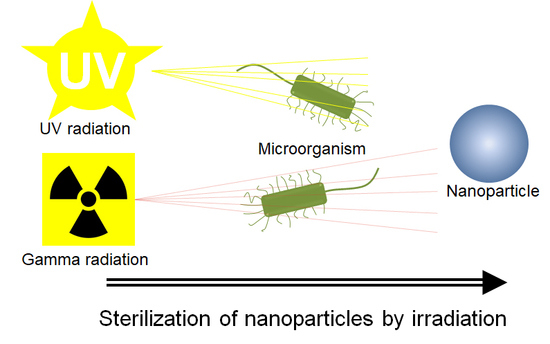
1. Giới thiệu
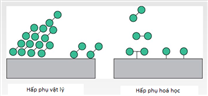
Các hạt nano cao phân tử (NP) được ứng dụng rộng rãi trong ngành dược phẩm và y sinh. NP đã được coi là các hạt keo rắn có kích thước từ 1 đến 1000 nm và bao gồm các vật liệu cao phân tử trong đó hàng hóa (thuốc hoặc phân tử sinh học) được hòa tan, nguyên tắc hoạt động là bị hấp phụ hoặc gắn vào. Chúng có thể kết hợp nhiều loại thuốc và phân tử vào các mô khác nhau với khả năng tương thích sinh học cao, khả năng phân hủy sinh học, độc tính thấp và kéo dài thời gian giải phóng. Poly- (ε-caprolactone) (PCL) và poly- ( D , L -lactic-axit co -glycolic (PLGA) là hai trong số các chất nền hiệu quả nhất cho các hạt nano, có thể được sản xuất với các hình dạng và kích thước khác nhau với khả năng tái tạo cao. Nhiều hệ thống phân tử nano đã được phát triển để được sử dụng làm phương tiện dược lý hoặc vectơ liệu pháp gen cho một số mô như phân phối hệ thần kinh trung ương (CNS) có thể được tạo thành của các polyme kỵ nước như poly (axit lactic) (PLA), PLGA và PCL.
Tính hữu dụng của các công thức NP này và ý nghĩa y tế đối với việc sử dụng in vivo của chúng đòi hỏi các điều kiện sản xuất vô trùng. Theo Dược điển Hoa Kỳ (USP), các công thức NP phải vô trùng; tuy nhiên, các nghiên cứu nhằm xác định các điều kiện khử trùng NP mới hiện vẫn chưa đủ. Về vấn đề này, một số phương pháp khử trùng đã được áp dụng, bao gồm nhiệt, phương pháp hóa học, lọc và khử trùng bằng ion hóa. Tuy nhiên, đối với NP cao phân tử, một số kết quả trong số này, mặc dù hiệu quả, nhưng gây ra những thay đổi trong các đặc tính hóa lý. Masson và cộng sự đã phân tích khử trùng bằng nhiệt, bức xạ gamma và lọc trong hệ thống NP dựa trên PCL với các chất hoạt động bề mặt khác nhau, nhận thấy rằng chỉ lọc không ảnh hưởng đến các đặc tính vật lý của hệ thống. Tuy nhiên, kích thước NP yêu cầu nhỏ hơn 220 nm trong chất lỏng không nhớt.
Những phát hiện này chứng minh rằng quá trình khử trùng bằng nhiệt dẫn đến kết tụ và thay đổi màu sắc, chứng tỏ có nhiều thay đổi về cấu trúc. Liên quan đến bức xạ gamma, khử trùng với 25 kGy làm tăng trọng lượng phân tử của polyme trong NP do sự hình thành các gốc và liên kết chéo giữa các chuỗi polyme và thậm chí giữa chất hoạt động bề mặt và chuỗi polyme. Một chiến lược phân tích tương tự đã được thực hiện trong hệ thống NP PLGA (52:48). Sau khi khử trùng bằng chiếu xạ gamma (25 kGy), không có sự khác biệt có ý nghĩa thống kê nào về kích thước hạt trung bình và thế Z; tuy nhiên, chỉ số polydispersity (PDI) tăng đáng kể. Việc thu được các phân tán đồng nhất rất phức tạp, và việc giải phóng thuốc bị ảnh hưởng tiêu cực trong NP tiệt trùng. Mặt khác, Shahabi et al. đã sử dụng tổ hợp PLGA (80:20) -PEG / hydroxyapatite để phân tích tác động của các liều lượng bức xạ gamma khác nhau, xác nhận sự giảm đáng kể trọng lượng phân tử polyme do hiện tượng cắt chuỗi.
Năm 2005, Bozdag và.al., đã đánh giá ảnh hưởng của việc khử trùng bằng bức xạ gamma đối với các đặc tính của các hạt nano poly ( D , L -lactide-glycolide) được nạp ciprofloxacin HCl. Kết quả thu được cho thấy việc giải phóng thuốc bị ảnh hưởng tiêu cực sau khi chiếu xạ gamma. Ngoài những kết quả này, tác dụng của các hạt nano đối với vi sinh vật là rất phù hợp. Tương tự, năm 2006, Memisoglu-Bilensoy E. et al. đã xây dựng các hạt nano cyclodextrin và đánh giá sự thay đổi của một số đặc tính, bao gồm cả việc bao bọc và phân phối thuốc, do quá trình khử trùng khác nhau. Họ đã chứng minh rằng những thay đổi quan sát được sau khi khử trùng bằng bức xạ gamma là không đáng kể so với những thay đổi quan sát được sau khi khử trùng bằng hấp và lọc. Các báo cáo trước đây đã mô tả rằng mức độ chiếu xạ gamma cao có thể làm thay đổi cấu trúc giải phóng của thuốc; tuy nhiên, điều này phụ thuộc vào thành phần của cả polyme và chất hoạt động bề mặt của mỗi hệ thống hạt nano. Do đó, mặc dù chiếu xạ tia gamma sẽ mang lại hiệu quả khử trùng NP, nhưng các tác động hóa lý đối với hệ thống NP có thể còn nghi ngờ. Vì những lý do này, các chiến lược khử trùng nhanh chóng và hứa hẹn khác đã bắt đầu được áp dụng. Trong trường hợp khử trùng bằng tia cực tím (UV), có rất ít công trình ứng dụng trong NP. Trong các hệ thống ống nano và hạt kim loại, khử trùng bằng tia cực tím đã được sử dụng và được chứng minh là có hiệu quả để loại bỏ vi sinh vật, và không có thay đổi bất lợi nào được quan sát thấy. Nhìn chung, các phương pháp khác nhau được phân tích có nhược điểm trong các công thức NP. Vì vậy, cần phải tìm ra các điều kiện tiệt trùng tốt hơn mà không làm thay đổi các đặc tính hóa lý của NP. Thậm chí, hiệu quả khử trùng của chiếu xạ gamma liều thấp (8 và 13 kGy) đã được chứng minh khi có mặt một số đường bảo vệ như glucose và mannitol ở mức 5% trong chitosan hydrogel-NP. Thông thường, sự hiện diện của các chất bảo vệ lạnh với số lượng đáng kể trong các lô cuối cùng của NP, vì vậy việc xem xét tác dụng bổ sung của tá dược đó là hợp lý.
Do đó, trong nghiên cứu này, tác giả đã phân tích tác động của hai phương pháp khử trùng dựa trên chiếu xạ gamma thấp và tia UV lên hai loại hạt nano được mô tả rộng trong ứng dụng y tế (PCL và PLGA), với sự hiện diện của PVA như chất hoạt động bề mặt và chất bảo vệ lạnh. Quá trình khử trùng ở trạng thái rắn. Một phân tích hóa lý được thực hiện trước và sau khi khử trùng cũng như kiểm tra khả năng sống của tế bào trong một dòng tế bào thần kinh để xác định các tác động có thể xảy ra do bức xạ gamma và tia UV. Trong các điều kiện phân tích, ánh sáng UV được chứng minh là an toàn và hiệu quả, trong khi chiếu xạ gamma làm thay đổi một chút các thông số vật lý và có xu hướng làm tăng chết tế bào ở nồng độ NP cao.
2. Vật liệu và phương pháp
2.1. Nguyên vật liệu
Để xây dựng NP, nhóm nghiên cứu đã sử dụng poly-ε-caprolactone (Mn 14.000 g / mol), poly ( D , L -lactide- co -glycolide) (Mn 30.000-60.000 g / mol), Mowiol 4-88 (rượu polyvinyl 4-88) và D - (+) - trehalose dihydrate, được cung cấp bởi Sigma-Aldrich ® (Merck KGaA, Dramstadt, Đức), trong khi ethyl acetate được mua từ Spectrum ® (Spectrum Laboratory Products, NJ, USA). Mannitol được lấy từ Central de Drogas, SA de CV (Mexico City, Mexico). Đối với các thử nghiệm sinh học, tác giả sử dụng môi trường Eagle's (DMEM) đã được sửa đổi của Dulbecco, penicillin-streptomycin, trypsin-EDTA, PBS 1X và sodium pyruvate, được lấy từ Gibco ®/ Life Technologies (ThermoFisher Scientific, MA, USA); huyết thanh bò thai (FBS) được cung cấp bởi Biowest ® (Nuaillé, Pháp), trypan blue và paraformaldehyde P6148 được cung cấp bởi Sigma-Aldrich ® (Merck KGaA, Dramstadt, Đức) và Bộ tăng sinh tế bào I (MTT) được mua từ Roche ® (Roche Diagnostics GmbH, Mannheim, Đức).
2.2. Chuẩn bị hệ thống hạt nano
PCL / PVA NP và PLGA / PVA NP thu được thông qua phương pháp khuếch tán-nhũ tương như đã báo cáo trước đây. Tóm lại, etyl axetat được trộn với nước cất hai lần (QGARD00R1, Merck Millipore ® , Dramstadt, Đức), theo tỷ lệ 1: 1, để tạo ra các pha bão hòa (pha bão hòa hữu cơ — OSP, và pha bão hòa nước — ASP) . Đối với PCL / PVA NP, 400 mg PCL được hòa tan trong OSP để thu được dung dịch 2% ( w / v ). Hỗn hợp được thêm vào PVA trong ASP (5% w / v ), và sau đó nó được nhũ hóa bằng thiết bị đồng hóa tốc độ cao (Ultra Turrax T18 IKA ®; Wilmington, NC, USA) ở tốc độ 11.000 vòng / phút trong 10 phút ở nhiệt độ phòng. Sau đó, môi trường khuếch tán (nước ở cùng nhiệt độ) được thêm vào. Dung môi hữu cơ được làm bay hơi bằng chân không (Heidolph ® Instruments GmbH & Co., KG, Schwabach, Đức). Hỗn dịch NP thu được chỉ được ly tâm một lần ở tốc độ 11.000 vòng / phút trong 90 phút ở 4 ° C (Máy ly tâm model 5804 R; Eppendorf ® , Hamburg, Đức). Cuối cùng, viên nén được ngâm lại trong nước cất. Đối với hệ thống tiếp theo, PLGA / PVA NP được chuẩn bị với quy trình tương tự ngoại trừ việc PLGA được hòa tan trong OSP ở mức 1% ( w / v), và giải pháp của PVA được sử dụng ở mức 2,7% (W / V) trong ASP. Các công thức được đông lạnh và đông khô (49 ° C, 0,05 mBar, và 24 giờ). Đối với NP PCL / PVA, 20% D - (+) - trehalose được hòa tan trong 70 mg / mL PCL / PVA NP, trong khi 15% mannitol được hòa tan trong 56,45 mg / mL PLGA / PVA NP. Đầu tiên NP được đông lạnh ở -20 ° C trong thiết bị siêu đông Thermo Scientific trong 18 giờ, và sau đó, các hệ thống đông lạnh được đông khô ở -45 ° C trong 2 giờ, ở độ dốc 1 ° C / phút như trong báo cáo trước đó của Abdelwahed W và cộng sự.
2.3. Phương pháp khử trùng
Cả hai hệ thống NP đều được khử trùng bằng hai phương pháp khác nhau, chiếu tia UV và tia gamma, để đánh giá những thay đổi hóa lý có thể có trong NP sau quá trình xử lý. Đối với chiếu xạ UV, NP đông khô (1 mg) và NP ở trạng thái phân tán trong nước (1 mg / mL) với độ nhớt 110 cP (môi trường nhớt), được đặt trong các ống vi ly tâm 1,5 mL (ống Eppendorf 3810X; Eppendorf, Hamburg, Đức) và được khử trùng bằng bức xạ UV trong các thời gian tiếp xúc khác nhau (0,5, 1,0, 1,5, 2, 2,5 và 3 giờ) bằng thiết bị liên kết ngang tia cực tím UVC 500 (Amersham Biosciences ® , UA) với liều 100 µJ / cm2, trong khi đối với chiếu xạ gamma, các lọ thủy tinh chứa đầy NP (20 × 55 mm) được đóng gói trong túi khử trùng kép và được chiếu xạ trong không khí, liều gamma 5 và 10 kGy ở tốc độ liều 125 Gy / phút, sử dụng máy chiếu xạ chùm tia Gamma 651PT với một nguồn Co tia gamma (AECL ® , năng lượng nguyên tử của Canada Ltd, Ottawa, Canada). Cả hai quy trình được thực hiện ở nhiệt độ phòng. Các thí nghiệm này được lặp lại ít nhất ba lần.
2.4. Đánh giá vi sinh
Sau khi chuẩn bị hệ thống NP, chúng được phân tán (1 mg / mL) bằng phương pháp khuấy cơ học, và sau đó 100 µL NP được cấy với sự khuếch tán xuyên tâm trên bề mặt của môi trường nuôi cấy. Đĩa thạch huyết cừu 5% và đĩa thạch MacConkey dùng để đếm vi khuẩn và coliform, trong khi đĩa thạch Saboroud dextrose dùng để đếm nấm và được ủ ở 35 ° C và phân tích sau 24 giờ trong 7 ngày. Số lượng vi sinh vật được báo cáo là số lượng đơn vị hình thành khuẩn lạc (CFU / mL). Để xác định vi sinh vật sống sót, phương pháp nhuộm Gram được thực hiện để phân loại chúng theo các đặc điểm do thành vi khuẩn quy định. Để phân tích chi tiết, trực khuẩn Gram âm (GN) đã được kiểm tra bằng phản ứng indole và oxidase. Trong khi đó, đối với cầu khuẩn Gram dương (GP), Các thử nghiệm catalase và coagulase đã được tiến hành. Để xác định đầy đủ các vi sinh vật, Hệ thống VITEK 2 (bioMérieux, Marcy d'Etoile, Pháp) đã được sử dụng.
Mặt khác, hiệu quả của quá trình tiệt trùng được đánh giá bằng cách thử độ vô trùng của các mẫu bị nhiễm bẩn trước khi chiếu xạ với huyền phù của Escherichia coli ATCC 25922, Staphylococcus aureus ATCC 29213 và Candida albicans ATCC 10231. Nồng độ 1 × 10 8CFU / mL của các chủng được phân tích trong mỗi lọ có chứa mỗi một NP polyme, và 0,5 mL chất cấy được thêm vào 0,5 mL phân tán NP. Trước khi chiếu xạ, các lọ được đậy kín bằng nút cao su. Sau khi chiếu xạ, phần mẫu được cấy vào các đĩa thạch khác nhau và các đầu dò sinh hóa, được mô tả trước đây. Các vi sinh vật sống sót được đếm sau 24 giờ ủ ở 35 ° C trong 7 ngày và được báo cáo là số lượng đơn vị hình thành khuẩn lạc (CFU / mL).
2.5. Đặc tính hóa lý
2.5.1. Kích thước hạt và Đo lường Zeta-Tiềm năng
Kích thước hạt, sự phân bố (được gọi là chỉ số phân tán, PDI) và tiềm năng zeta được xác định bằng cách sử dụng Malvern Zetasizer Nano (Malvern Instruments model ZS90; Malvern, UK). Kích thước hạt và PDI được đo bằng tán xạ ánh sáng động (DLS), trong khi điện thế zeta được đo bằng doppler laser đo vận tốc (VLS). Các phép đo được thực hiện sau quá trình đông khô ở 25 °C. Để đánh giá hóa lý, hệ thống NP đông khô được đình chỉ lại ở 1 mg / mL thông qua khuấy cơ học ở 3000 vòng / phút trong 1 giờ (Model MS 3 digital, IKA Works Inc., USA). Mỗi giá trị là kết quả của các phép xác định trong ba lần. Do đó, kết quả được báo cáo dưới dạng trung bình ± độ lệch chuẩn (SD).
2.5.2. Kính hiển vi điện tử quét (SEM)
Hình thái của NP đông khô được kiểm tra bằng phương pháp hiển vi điện tử quét (SEM) sử dụng kính hiển vi điện tử quét phát xạ trường (Model JSM-7600F; Công ty Jeol, Nhật Bản). Trước khi đánh giá, các mẫu đã được chuẩn bị trên kính che và phủ vàng, trong môi trường khí argon, bằng máy phun phún ion (Model JFC-1100, Jeol Company Japan).
2.5.3. Quang phổ Fourier Transform-InfraRed (FTIR)
Để đánh giá các tương tác hóa học sau quá trình khử trùng, NP đông khô và thuốc thử được phân tích bằng quang phổ hồng ngoại biến đổi Fourier (FITR) sử dụng quang phổ FTIR Nicolet 6700 (Thermo Scientific, Waltham, MA, USA). Phạm vi quét là 4000–400 cm −1 , và độ phân giải là 2 cm −1 .
2.5.4. Phân tích đo nhiệt độ (TGA)
TGA đã đánh giá độ ổn định nhiệt của NP, khi có và không có quá trình khử trùng. Tóm lại, các mẫu đông khô khoảng 5 mg đã được thử nghiệm trong Máy phân tích nhiệt kế Hi-Res TGA 2950 (TA Instruments, Inc., DE, USA). Các thử nghiệm được thực hiện trong môi trường nitơ, từ nhiệt độ phòng đến 500 ° C và ở tốc độ gia nhiệt 10 ° C / phút.
2.5.5. Nhiệt lượng quét vi sai (DSC)
Việc đánh giá các đặc tính nhiệt NP được thực hiện bởi DSC. Các mẫu NP đông khô trước và sau quá trình khử trùng được kiểm tra trong các ô nhôm kín bằng DSC 2910 (Modulated TA Instruments, Inc., DE, USA) trong môi trường nitơ, từ nhiệt độ phòng đến 250 ° C và ở nhiệt độ nóng tốc độ 10 ° C / phút.
2.6. Đặc tính sinh học
2.6.1. Nuôi cấy tế bào
Để phân tích tác dụng của phương pháp khử trùng trong nuôi cấy tế bào, chúng tôi chọn dòng tế bào có hệ thần kinh trung ương (CNS) ở người có ký hiệu là Müller glial (dòng tế bào MIO-M1). Tế bào được cung cấp bởi Tiến sĩ Arturo Ortega từ CINVESTAV-IPN, Mexico. Tế bào được duy trì dưới dạng nuôi cấy đơn lớp trong DMEM và được bổ sung 10% FBS và 1% penicillin / streptomycin, ở 37 ° C và 5% CO 2 trong môi trường được làm ẩm hoàn toàn. Môi trường nuôi cấy tế bào được làm mới sau mỗi 48 giờ. Khi các tế bào tiếp cận với 80% hợp lưu, chúng được trypsinized và nuôi cấy phụ trong môi trường tăng trưởng và được sử dụng để kiểm tra khả năng sống.
2.6.2. Thử nghiệm khả năng tồn tại của tế bào
Độc tính tế bào in vitro của NP, trước và sau quá trình khử trùng, được xác định bằng cách sử dụng Bộ công cụ tăng sinh tế bào I (Roche Diagnostics GmbH, Mannheim, Germany) với dòng tế bào MIO-M1. Một cách ngắn gọn, các tế bào được cấy trên đĩa 96 giếng 24 giờ trước khi thử nghiệm. Sau đó, các tế bào được ủ với môi trường tươi (150 µL), bao gồm các nồng độ khác nhau của NP không khử trùng và NP đã khử trùng (UV, 5 và 10 kGy, nồng độ: 10, 20, 30, 60, 80, 100, 150 và 200 µg / mL) trong 24 giờ (6000 tế bào / giếng), 48 giờ (4000 tế bào / giếng) và 72 giờ (1800 tế bào / giếng). Các tế bào được ủ với chỉ DMEM được gọi là tế bào chưa được xử lý và kiểm soát với 0,1 M H 2 O 2. Sau đó, các tế bào được rửa hai lần bằng PBS 1X. Sau đó, 10 µL dung dịch 3 - (4,5-DiMetylThiazol-2-yl) -2,5-diphenyl tetrazolium bromua (MTT) (5 mg / mL) được thêm vào mỗi giếng, và các đĩa được ủ ở 37 ° C trong 4 giờ trong môi trường ẩm. Sau đó, dung dịch hòa tan cho mỗi giếng được thêm vào và ủ qua đêm để hòa tan các tinh thể muối hình thành. Sản phẩm formazan được định lượng bằng phương pháp đo quang phổ bằng đầu đọc vi tấm đa chế độ Synergy HTX (BioTek ® , Vermont, Hoa Kỳ) ở bước sóng 570 nm. Tất cả các thí nghiệm được sắp xếp thành ba lần để phân tích thống kê. Kết quả được biểu thị bằng giá trị trung bình ± SD.
2.6.3. Phân tích miễn dịch huỳnh quang và kính hiển vi đồng tiêu
Các phân tích nhuộm miễn dịch và CLSM được thực hiện theo các kỹ thuật tiêu chuẩn. Một cách ngắn gọn, các tế bào MIO-M1 (12.000 tế bào) đã được gieo hạt trong các đĩa nuôi cấy mô có chứa các tấm bìa và được ủ trong 24 giờ. Tế bào được rửa hai lần bằng PBS, và xử lý bằng PCL / PVA hoặc PLGA / PVA NP được bổ sung ở nồng độ 80 µg / mL hoặc 200 µg / mL mà không cần khử trùng, chiếu tia UV, hoặc chiếu xạ gamma 5 hoặc 10 kGy trong 48 giờ. Sau thời gian ủ, tế bào được rửa hai lần bằng PBS và cố định bằng 4% paraformaldehyde trong PBS trong 20 phút. Sau khi cố định, tế bào được rửa hai lần và làm thấm với 2% triton X-100 trong PBS trong 5 phút. Sau đó, chúng được rửa hai lần và chặn bằng 0,5% gelatin và 1,5% FBS trong PBS trong 20 phút. Sau đó, các tế bào được đánh dấu bằng kháng thể chính phalloidin (Phòng thí nghiệm nghiên cứu miễn dịch Jackson), và rửa hai lần bằng PBS. Bìa mềm được gắn trong các trang trình bày với VectaShield / DAPI (Vectorlabs® ) và được niêm phong. Hình ảnh được thu thập bằng hệ thống laser đồng tiêu TCS-SP5 (Leica Microsystems, Đức).
Xem thêm: Ảnh hưởng của quá trình khử trùng bằng tia UV và bức xạ gamma đối với các hạt nano polyme khác nhau cho các ứng dụng y sinh (Phần 2)